Hugo POINSIGNON*,**, Patrick HENRY**, Jean-Guillaume DILLINGER**, *Service de cardiologie, hôpital Robert-Debré, CHU de Reims, **Département de cardiologie, hôpital Lariboisière, AP-HP, Paris
Les nouvelles recommandations « Management of cardiovascular disease in patients with diabetes »(1), publiées lors de l’ESC en août 2023, offrent une synthèse sur la prise en charge moderne du diabète en 2023, depuis sa prévention et sa détection, jusqu’au traitement de ses complications. Pour les patients diabétiques sans complication, le SCORE2-Diabète apparaît pour évaluer le risque cardiovasculaire (CV) de ces patients. Les recommandations insistent largement sur le dépistage et le traitement de 3 principales complications liées au diabète (figure 1) : la maladie athéromateuse, l’insuffisance cardiaque (IC) et enfin la maladie rénale chronique (MRC). Ces nouvelles recommandations renforcent la place du cardiologue dans la prise en charge du patient diabétique, notamment de type 2, et de toutes ses complications pour améliorer son pronostic et sa qualité de vie.
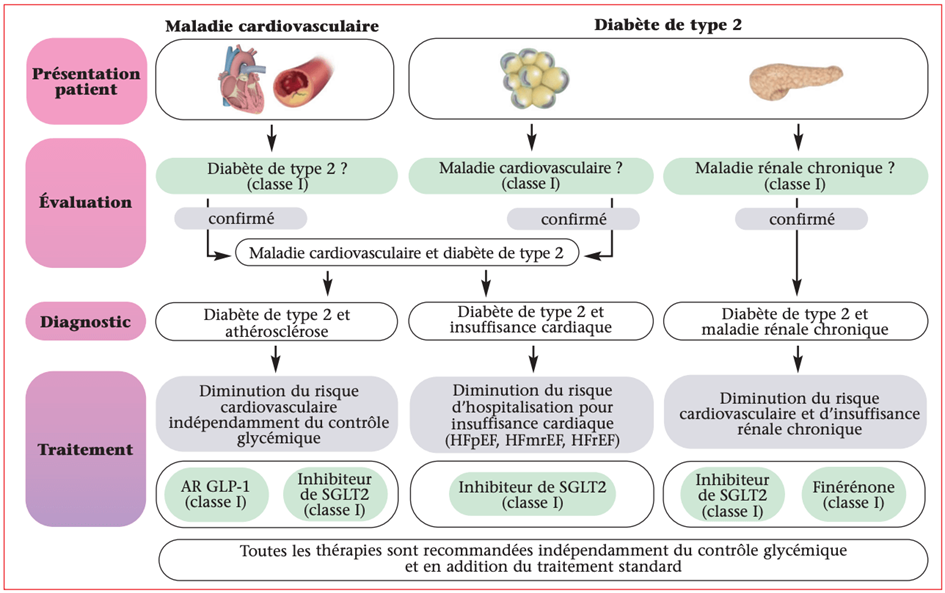
Figure 1. Prise en charge de la maladie cardiovasculaire chez les patients diabétiques de type 2 : approche clinique et recommandations clés (adapté à partir de la figure centrale publiée dans les recommandations ESC 2023).
Points clés
• Dans le diabète de type 2 sans complication : intérêt d’un nouveau score de stratification du risque, le SCORE2-Diabète évaluant le risque de maladie cardiovasculaire (CV) à 10 ans.
• Place majeure des derniers traitements tels que les iSGLT2, les agonistes du GLP-1 et la finérénone. En première intention en fonction du type de complications du diabète : maladie athéromateuse, insuffisance cardiaque (IC) ou maladie rénale chronique (MRC).
Diagnostic du diabète et du prédiabète
Les recommandations soulignent une nouvelle fois la prévalence encore beaucoup trop élevée de patients diabétiques non diagnostiqués.
Voici les principaux tests et leur valeur pour établir le diagnostic de diabète :
– glycémie à jeun ≥ 7,0 mmol/L (≥ 1,26 g/L) sur 2 prélèvements différents en l’absence de symptôme ;
– glycémie ≥ 11,1 mmol/L (2,0 g/L) sur un seul prélèvement ;
– glycémie ≥ 11,1 mmol/L (2,0 g/L) 2 heures après hyperglycémie orale provoquée (HGPO) par l’administration de 75 g de glucose ;
– HbA1c ≥ 6,5 %.
Les valeurs seuils pour le diagnostic de prédiabète demeurent toujours controversées, définies par une glycémie à jeun à 6,1- 6,9 mmol/L (1,10-1,26 g/dL) selon la WHO et 5,6-6,9 mmol/L (1,0-1,26 g/dL) selon l’ADA. Par ailleurs, on peut également parler de prédiabète en cas de glycémie à 7,8-11,0 mmol/L (1,40-1,99 g/dL) après HGPO ou d’HbA1c entre 6,0 et 6,4 % (voire 5,7-6,4 % selon l’ADA).
Concernant le dépistage du diabète, tous les patients porteurs d’une maladie CV doivent être dépistés, de préférence par une glycémie à jeun ou un dosage de l’HbA1c (classe I, A). L’HGPO garde une place en cas de doute diagnostique (I, B).
Stratification du risque cardiovasculaire
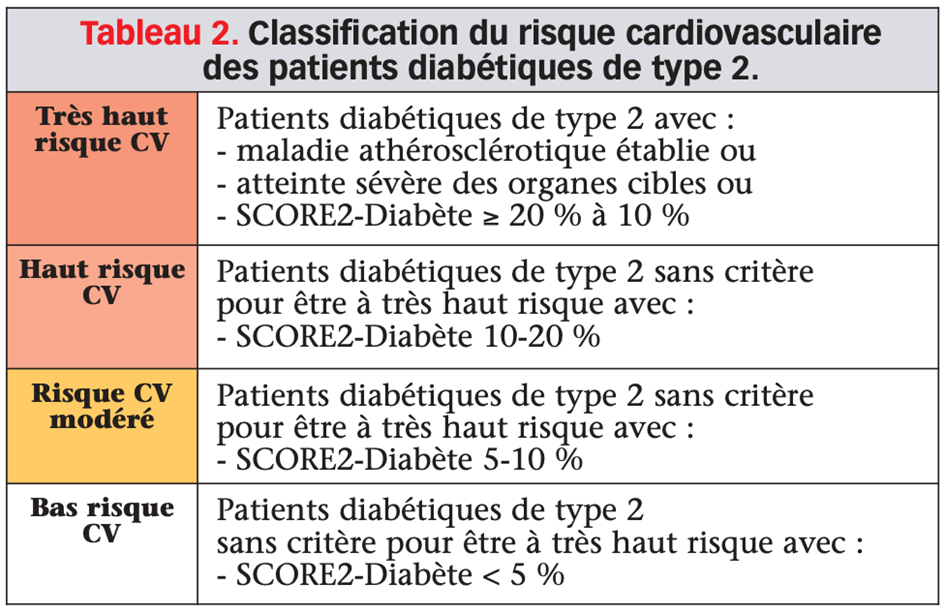
Compte tenu du pronostic CV péjoratif des patients diabétiques de type 2 (DT2) avec un risque 2 à 4 fois plus élevé de développer un événement, ces recommandations insistent sur la stratification du risque CV via l’introduction d’un nouveau score : SCORE2-Diabète (I, B), mieux adapté aux patients diabétiques. Ce nouveau score ne s’applique pas aux patients diabétiques avec une maladie athéromateuse avérée ou avec une atteinte sévère d’organes cibles (tableau 1) qui sont d’emblée classés à très haut risque CV (risque d’événements CV ≥ 20 % à 10 ans). Chez les autres patients, le SCORE2-Diabète permet d’estimer le risque d’événement CV fatal et non fatal à 10 ans (décès CV, infarctus du myocarde, accident vasculaire cérébral) à partir des facteurs de risque cardiovasculaires (âge, fumeur actif, pression artérielle systolique, cholestérol total et HDL-cholestérol), mais aussi d’informations concernant le diabète (âge au diagnostic, HbA1c, clairance de créatinine). L’objectif principal de ce score (disponible sur l’application ESC CVD Risk Calculation) est donc de mieux personnaliser la prise en charge des patients diabétiques en prévention primaire et ainsi guider les cliniciens dans leur pratique quotidienne.
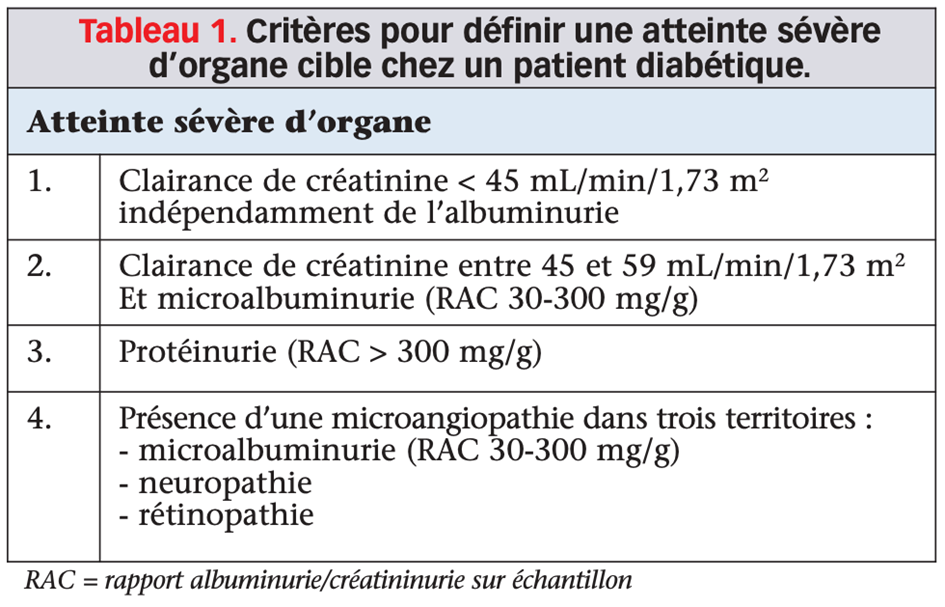
Il est donc essentiel pour stratifier le risque CV (tableau 2) de rechercher une atteinte d’organes cibles ou de symptômes faisant suspecter une atteinte athéromateuse (classe I, A) et en leur absence de calculer le score de risque du patient (SCORE2- Diabète).
Prise en charge de la maladie coronaire
Les recommandations rappellent que le diabète, facteur de risque pronostique bien établi de coronaropathie, a une prévalence de 25 % chez les patients avec un syndrome coronarien aigu (SCA). Le diabète doit donc être soigneusement recherché chez tout patient admis pour SCA.
Les recommandations actuelles ne reviennent pas sur la stratégie de dépistage de la maladie coronaire, dont la dernière mise à jour remonte aux recommandations ESC 2019.
En revanche, elles insistent à nouveau sur l’importance d’utiliser en première intention des traitements antidiabétiques avec bénéfice CV démontré (figure 2).
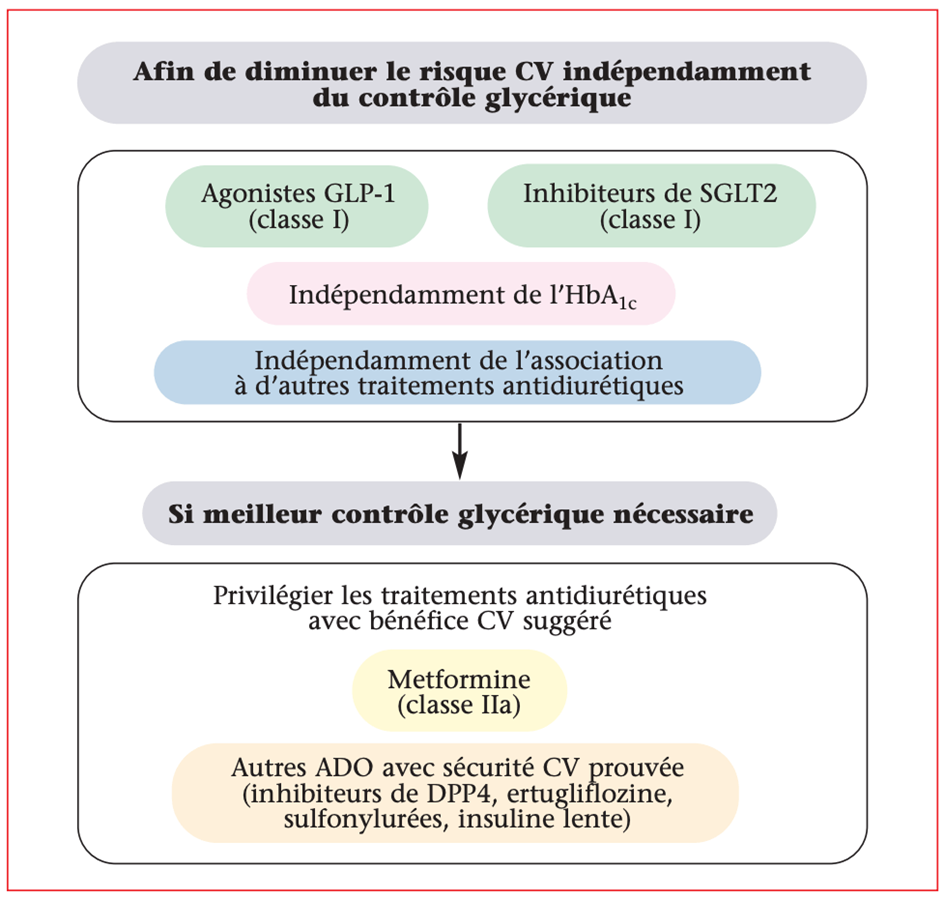
Figure 2. Stratégie thérapeutique antidiabétique chez les patients diabétiques de type 2 porteurs d’une maladie CV athéromateuse (adapté à partir des recommandations ESC 2023).
Les inhibiteurs du co-transporteur sodium-glucose 2 (iSGLT2) et les agonistes des récepteurs glucagon-peptide-1 (GLP-1) doivent donc être privilégiés chez les patients diabétiques avec coronaropathie ou athérosclérose afin de diminuer les événements CV indépendamment de l’HbA1c (I, A).
Concernant la revascularisation, le pontage coronaire avec greffon artériel doit être privilégié à l’angioplastie complexe chez les patients diabétiques avec atteinte pluritronculaire (atteinte du tronc commun, Syntax score > 22), en tenant compte des caractéristiques du patient (fragilité, maladie cérébrovasculaire, etc.). Il est recommandé d’utiliser les mêmes techniques de revascularisation (type de stent, abord radial pour l’angioplastie et utilisation de l’artère mammaire interne gauche comme greffon pour le pontage) chez les diabétiques et chez les non-diabétiques (I, A).
Concernant la coronaropathie stable, la revascularisation est recommandée comme chez le non-diabétique, en cas de symptomatologie angineuse persistante malgré un traitement antiangineux ou avec territoire ischémique > 10 % (I, A).
Dans le STEMI, après le traitement de l’occlusion coronaire aiguë, une revascularisation complète est préconisée sur les lésions coronaires non coupables (I, A). La revascularisation complète doit également être privilégiée dans le NSTEMI (IIa, C), mais pas dans le choc cardiogénique (III, B).
Concernant la stratégie antithrombotique, les recommandations sont les mêmes que dans la population générale. À noter que la double antiagrégation plaquettaire peut-être poursuivie pendant 3 ans (au-delà des 12 mois post-IDM) si le traitement a été bien toléré sans complication hémorragique majeure (IIa, A).
Il est par ailleurs rappelé l’importance d’évaluer le statut glycémique à l’admission de tout SCA (I, B), qui est corrélé aux événements intrahospitaliers indépendamment du statut diabétique. Le monitorage glycémique chez les patients diabétiques connus ou avec hyperglycémie est donc essentiel (I, C), avec instauration d’un traitement hypoglycémiant en cas d’hyperglycémie > 2,0 g/L (IIa, C).
Prise en charge de l’insuffisance cardiaque
L’IC est une des manifestations initiales les plus courantes de la maladie CV chez les patients diabétiques. Elle peut se présenter sous ses 3 formes : IC à fraction d’éjection du ventricule gauche préservée (HFpEF), modérément altérée (HFmrEF) ou réduite (HFrEF). Les causes principales d’IC chez ces patients sont multiples : la présence d’une cardiopathie ischémique sous-jacente, une HTA ancienne, les effets directs ou indirects de l’hyperglycémie, l’obésité, une FA plus fréquente et les autres facteurs CV associés. Le diabète est donc un facteur de risque important d’IC et il faut rechercher les symptômes faisant suspecter une IC régulièrement, à chaque évaluation médicale chez tout patient diabétique (I, C).
Dans ces nouvelles recommandations, il est souligné l’importance de la quadrithérapie (« les 4 fantastiques ») associant les iSGLT2, le sacubitril/valsartan ou IEC, les bêtabloquants et les inhibiteurs des minéralocorticoïdes chez les patients avec HFrEF, afin de diminuer le risque de mortalité et d’hospitalisation pour IC (I, A). L’accent est également mis sur la rapidité de titration de cette quadrithérapie puisqu’un délai de 6 semaines est préconisé afin d’atteindre les doses maximales tolérées (I, A).
La place de l’ivabradine, de la digoxine ou des dispositifs tels que les DAI ou CRT-D/P reste la même.
À noter que l’hydralazine ou les dérivés nitrés peuvent être utilisés chez les patients d’ethnie noire diabétiques en cas de FEVG < 35 % ou de FEVG < 45 % avec un VG dilaté, restant symptomatique en classe NYHA II-IV malgré la quadrithérapie classique (IIa, B).
Ainsi, voici les recommandations concernant les traitements antidiabétiques dans l’IC :
– les iSGLT2 sont recommandés chez les patients DT2 avec de nombreux facteurs de risque CV ou avec maladie CV avérée, afin de diminuer le risque d’IC (I, A) ;
– les iSGLT2 sont recommandés chez les DT2 avec HFrEF, afin de diminuer le risque de mortalité CV et d’hospitalisation pour IC (I, A) ;
– les iSGLT2 sont recommandés chez les patients diabétiques en cas d’IC même en cas de FEVG > 40 % (I, A) ;
– les agonistes GLP-1, les iDPP4 (sitagliptine, linagliptine), l’insuline lente et la metformine ont un effet neutre démontré sur le risque d’IC, et peuvent donc être considérés en seconde intention si nécessaire afin d’améliorer l’équilibre glycémique chez les patients DT2 insuffisants cardiaques ou à risque d’insuffisance cardiaque (IIa, A/B) ;
– en revanche, la pioglitazone (thiazolidinediones) et la saxagliptine (iDPP4) sont contre-indiquées chez ces patients à risque en raison d’une augmentation du taux d’hospitalisation pour IC (III, A/B) ;
– il est donc recommandé de remplacer les médicaments antidiabétiques par des molécules avec bénéfice CV prouvé (I, C).
Prise en charge de la maladie rénale chronique
Une partie importante des recommandations est dédiée à la maladie rénale chronique (MRC), avec pour objectif de diminuer son impact majeur en termes de morbi-mortalité. Il est rappelé l’importance du dépistage de la MRC en routine par le calcul de la clairance de la créatinine, mais aussi du rapport albuminurie/créatinurie (RAC) qui peut être fait sur un échantillon d’urine. Le RAC est mis en avant comme marqueur précoce de néphropathie diabétique, facteur prédictif d’insuffisance rénale chronique (IRC) et de maladie CV indépendamment de la clairance de créatinine (tableau 1).
Sur le plan thérapeutique, la prise en charge globale du diabète et de la MRC intègre évidemment le contrôle de l’hypercholestérolémie, de la pression artérielle (objectif PA < 130/80 mmHg) et des autres facteurs de risque cardiovasculaires (I, A). La dose maximale tolérée d’IEC ou d’ARA2 est toujours recommandée (I, A). Les iSGLT2 ont également leur place en cas de clairance de la créatinine > 20 mL/min, afin de réduire le risque de maladie CV et d’IRC (I, A).
La grande nouveauté de ces recommandations est l’introduction du nouvel antagoniste des récepteurs minéralocorticoïdes non stéroïdiens, la finérénone en association aux IEC/ARA2 en cas de clairance de la créatinine > 60 mL/min avec un RAC ≥ 300 mg/g ou en cas de clairance de la créatinine entre 25-60 mL/min avec un RAC > 30 mg/g, afin de réduire le risque d’événement CV et d’IRC (I, A).
Les agonistes GLP-1 peuvent être utilisés jusqu’à la clairance de la créatinine > 15 mL/min avec un bénéfice démontré sur la réduction du poids, du risque CV et de l’albuminurie (I, A).
Prise en charge du risque rythmique
La détection de fibrillation atriale (FA) chez les patients diabétiques reste fondamentale, car la FA est très fréquente et a des conséquences cliniques importantes. Le risque d’AVC lié à la FA est nettement plus élevé chez les patients diabétiques. Ainsi, un dépistage opportuniste par prise du pouls ou ECG est recommandé chez tous les patients diabétiques ≥ 65 ans (I, B). Ce dépistage doit être élargi aux patients < 65 ans, d’autant plus s’il existe d’autres facteurs de risque CV (I, C).
L’anticoagulation orale est recommandée chez les patients diabétiques en FA ayant un autre facteur de risque additionnel parmi le CHA2DS2-VASc (I, A) et peut être considérée même en l’absence d’autres facteurs de risque (IIa, B). Les anticoagulants oraux directs doivent être privilégiés sauf chez les patients porteurs d’une valve mécanique ou d’un rétrécissement mitral modéré à serré (I, A). Par ailleurs, les recommandations rappellent que les patients diabétiques sont également à plus haut risque d’arythmie ventriculaire et donc de mort subite, pouvant être favorisés par une cardiopathie sousjacente, mais aussi par l’hyperglycémie ou l’hypoglycémie. L’objectif est de détecter précocement une pathologie cardiaque sous-jacente via l’évaluation régulière des facteurs de risque et l’instauration d’un suivi cardiologique. Cependant, il n’y a pas de protocole de prise en charge spécifique chez ces patients.
Prise en charge de la maladie artérielle aortique et périphérique
L’atteinte artérielle périphérique (AOMI) fréquente chez les diabétiques est associée à un risque de mortalité multiplié par 2,5 à 5 ans. Le dépistage de l’AOMI est donc recommandé en routine par évaluation clinique ou par mesure de l’index de pression systolique (IPS) (I, C).
Un IPS < 0,90 fait porter le diagnostic d’AOMI, indépendamment des symptômes (classe I, C). En cas de symptômes, il est nécessaire de compléter les explorations par la réalisation d’un Doppler vasculaire (I, C). En cas d’IPS > 1,40, d’autres explorations doivent être envisagées comme le Doppler vasculaire ou la mesure de pression systolique à l’orteil (I, C).
Il est également recommandé d’évaluer le risque d’amputation chez tous les patients diabétiques avec ischémie critique des membres inférieurs, pouvant faire appel à la classification WIFI (wound, ischaemia, and foot infection) (I, B). Ce score comprend 4 niveaux pour chacun des 3 items (0 = pas, 1 = peu, 2 = moyen, 3 = sévère) et permet ainsi de prédire le risque d’amputation en différents niveaux de risque. L’éducation des patients atteints d’AOMI est donc essentielle, notamment la prévention, la détection précoce des ulcères et des signes d’infection (I, C).
Sur le plan thérapeutique, les objectifs de LDL et les indications de traitement antiagrégants plaquettaires restent les mêmes que chez tout patient à très haut risque CV (I, B). En cas d’ischémie critique, la revascularisation est à envisager à chaque fois que cela est possible pour le sauvetage du membre (I, C).
Une des nouveautés est la possibilité d’associer une faible dose de rivaroxaban (2,5 mg x 2/j) à l’antiagrégant plaquettaire chez les patients porteurs d’une AOMI symptomatique qui n’ont pas un risque hémorragique augmenté, ce qui permet de diminuer le risque d’événement CV incluant le risque d’amputation (IIa, B). Cependant, cette posologie de rivaroxaban n’existe pas en France et n’a pas encore l’AMM dans cette indication.
Concernant l’athérome carotidien et les anévrismes aortiques, la prise en charge des patients diabétiques doit être superposable à celle des patients non diabétiques (I, C).