Commercialisés depuis moins de 5 ans – mais pas en France ! – les inhibiteurs du cotransporteur Na+-glucose SGLT2 ont très rapidement trouvé une place de choix dans la boîte à outils des diabétologues qui, pourtant, s’étaient évertués à lutter contre la glycosurie pendant des lustres. De très nombreux essais cliniques randomisés contrôlés d’envergure ont eu raison du scepticisme initial d’une communauté diabétologique impressionnée par des effets pléiotropes (?) dépassant largement le cadre du contrôle de la glycémie.
La classe des gliflozines figure d’ores et déjà en bonne place, voire en première ligne pour certains, dans les recommandations de prise en charge du diabète les plus récentes. Cette revue générale fait l’inventaire des effets extraglycémiques d’une classe thérapeutique qui abaisse la glycémie en bloquant la réabsorption du glucose au niveau du tube proximal, indépendamment de l’action et de la disponibilité de l’insuline (tableau). Il en résulte une glycosurie estimée à 60 à 80 g de glucose par jour soit plus de 250 kcal/j associée à une diurèse osmotique et à une réduction de la pression artérielle. C’est à ces effets qu’ont été attribués initialement les bénéfices cardiovasculaires rapportés dans l’étude EMPA-REG OUTCOME datant de 2015, qui avait montré pour la première fois qu’un hypoglycémiant oral était à même de réduire la mortalité cardiaque et l’incidence des hospitalisations pour insuffisance cardiaque.
Ces effets bénéfiques confirmés par plusieurs essais cliniques sont encore imparfaitement expliqués. Ils ne tiennent pas à l’amélioration de la glycémie puisqu’ils sont retrouvés en l’absence de diabète et pourraient être liés à un effet intrinsèque sur la fonction ventriculaire gauche. Dans un modèle animal d’insuffisance cardiaque l’administration d’iSGLT2 réduit l’expression du TGF-β, du collagène I et II et la fibrose cardiaque. Les gliflozines réduisent l’albuminurie et freinent la détérioration de la fonction rénale. La perte de poids est constante mais limitée à 2 à 4 kg et se fait pour 60 à 70 % au détriment de la masse grasse, notamment de la graisse épicardique. La réduction de la pression artérielle, de 5 mmHg pour la systolique et de 2 mmHg pour la diastolique, est liée au fait que l’inhibition des réabsorptions du glucose et du sodium sont couplées. L’excrétion accrue des urates détermine une diminution de l’uricémie, bienvenue dans ce contexte puisque l’hyperuricémie est considérée par beaucoup comme un facteur de risque cardiovasculaire. Les modifications du profil lipidique comportent une augmentation du cholestérol-HDL et une diminution des triglycérides à la limite de la significativité. La stéatose hépatique et les marqueurs de cytolyse sont améliorés dans plusieurs études contrôlées. Il existe également une amélioration de la rigidité artérielle et de la fonction endothéliale. L’emploi des gliflozines semble à même de diminuer le stress oxydatif ainsi que l’inflammation en rééquilibrant les adipokines et les cytokines pro- et anti-inflammatoires. Enfin, ces molécules semblent avoir des propriétés de régénération vasculaire.
En revanche, la diminution des substrats glucosés assortie d’une élévation du rapport glucagon/insuline favorise la lipolyse et l’oxydation des acides gras et conduit à une production accrue de corps cétoniques pouvant être responsable d’une cétose euglycémique symptomatique. L’ensemble de ces effets extraglycémique semble être la conséquence d’un effet classe bien que certaines molécules se distinguent par des effets plus convaincants que d’autres dans certains domaines comme par exemple la canagliflozine sur l’évolution de l’insuffisance rénale.
Si les conséquences à long terme des effets extraglycémiques sont encore de l’ordre de la spéculation, il n’empêche que cette classe thérapeutique a une dimension supra-métabolique originale avérée qui justifie largement sa place dans la stratégie du traitement du diabète de type 2.
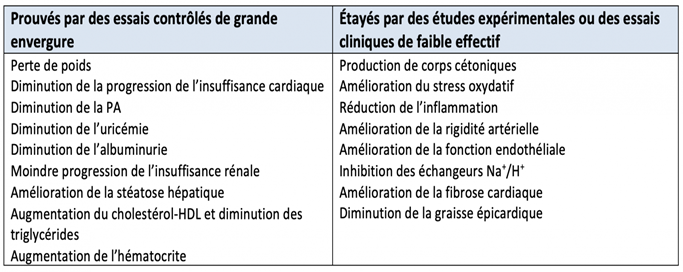
Tableau. Effets extraglycémiques des iSGLT2.
Jean-Louis SCHLIENGER, Strasbourg
Bonora BM et al. Extraglycemic effects of SGLT2 inhibitors: a review of the evidence. Diabetes Metab Syndr Obes 2020 ; 13 : 161-74.
